Überspannung
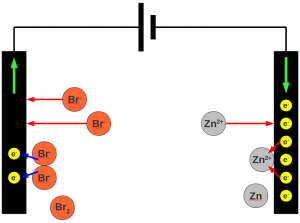
Elektrolysiert man wässrige Zinkbromidlösung, so verwendet man dazu in der Regel Graphitelektroden:
Dabei werden anodisch Brom (Pluspol) und kathodisch Zink (Minuspol) gebildet. Das ist jedoch keineswegs selbstverständlich, da an beiden Polen zwei verschiedene Reaktionen miteinander konkurrieren.
Kathode (Minuspol)
(1) Zn2+ + 2e- → Zn; UH0=-0,76V
(2) 2H2O + 2e- → H2 + 2OH-; UH0=-0,41V
Anode (Pluspol)
(3) 2Br- → Br2 + 2e- ; UH0=1,07V
(4) 2H2O → O2 + 4H+ + 4e- ; UH0=0,82V
Die Zersetzungsspannung von Wasser beträgt danach lediglich 1,23V, die von Zinkbromid 1,83V. Es wäre also zu erwarten, dass Wasserstoff und Sauerstoff gebildet werden. Tatsächlich erhält man bei Einsatz von platinierten Platinelektroden zumindest anstelle des Zinks Wasserstoff bei diesem Versuch.
Bei vielen Gasen stellt man fest, dass deren elektrolytische Gewinnung durch verschiedene Faktoren gehemmt ist und daher ein höheres als das theoretische berechnete Zersetzungspotential zu deren Gewinnung benötigt wird. Die Abweichung zwischen der theoretischen Zersetzungsspannung und dem tatsächlichen Wert bezeichnet man als Überspannung U*. Die Überspannung ist abhängig:
- vom Elektrodenmaterial
- von der Art des Gases
- von der Stromdichte
Dank der Überspannung des Wasserstoffs an Graphit beträgt das Potential der Halbzelle aus Gleichung (2) nicht 0,41V, sondern 0,41V + U*. In der Regel ist dieses Potential an der Graphitelektrode negativer als das des Zinks, weil bei Metallen in der Regel keine Überspannungseffekte auftreten.
Auch Sauerstoff besitzt an Graphit eine so große Überspannung, dass er unter normalen Umständen nicht gebildet wird – auch nicht mit platinierten Platinelektroden. Bei der Elektrolyse von Zinkbromidlösung mit Platinelektroden erhält man also Wasserstoff und Brom. Gleichzeitig sollte Zinkhydroxid ausfallen, da sich die Zinkionen mit den kathodisch gebildeten Hydroxidionen verbinden.
Die Überspannung des Wasserstoffs an Graphit macht diese Elektrolyse also überhaupt erst möglich.
Elektrolysiert man Natriumsulfatlösung, laufen dagegen tatsächlich die Prozesse (2) und (4) ab, da die Zersetzungsspannung von Natriumsulfat mit 4,7V sehr hoch ist. Färbt man die Lösung mit Universalindikator ein und elektrolysiert mit Platinelektroden, ergibt sich nach einer Weile folgendes Bild:
Fazit:
Der Stoff mit der geringeren Zersetzungsspannung bereinigt um den Überspannungsanteil wird bei Elektrolysen zuerst gebildet.