Warum Strukturformeln von Zuckermolekülen eigentlich keine Strukturformeln sind
Dazu muss man etwas ausholen. Ich beginne einmal mit Glycerin, dass sich durch folgende Strukturformeln darstellen lässt:
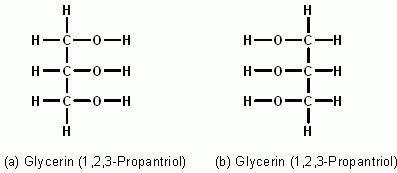
Beide Darstellungen sind absolut gleichwertig. Schließlich ist die C‑C-Einfachbindung frei drehbar, sodass sich die OH-Gruppen fast beliebig ausrichten können. Tatsächlich werden sie bevorzugt im Raum den größtmöglichen Abstand zueinander einnehmen, da das die energieärmste Form darstellt.
Bei einem Oxidationsprodukt des Glycerin, dem Glycerinaledhyd, sieht das etwas anders aus:
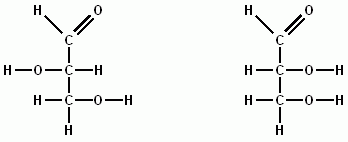
Um zu verstehen, wie es dazu kommt, dass hier von zwei verschiedenen Formen gesprochen wird, muss man die Moleküle etwas anders darstellen:
Versuche Sie einmal, mit der Maus beide Moleküle so zu drehen, das sie deckungsgleich nebeneinanderliegen. Es klappt natürlich nicht, aber woran liegt das?
Die beiden Molekülen sind Stereoisomere. Bedingt wird dies durch das mittlere C‑Atom, welches an jeder seiner vier Bindungsmöglichkeiten eine andere Gruppe, bzw. vier verschiedene Substituenten trägt. Ein derartiges C‑Atom wird asymmetrisches Kohlenstoffatom genannt.
Es macht also einen Unterschied, ob man bei asymmetrischen C‑Atomen in Zuckermolekülen die OH-Gruppe nach rechts oder nach links schreibt. Bloß wie kommt man man von der Strukturformel zum korrekten 3d-Molekülmodell?
Das ist sehr einfach:
Richten Sie die Aldehydgruppe nach oben aus. Drehen Sie das asymmetrische C‑Atome (es ist das C‑Atom in der Mitte) so, dass sowohl die OH-Gruppe als auch das Wasserstoffatom Ihnen „entgegenschauen“, also aus der Bildschirmebene hinausragen. Steht nun die OH-Gruppe rechts, muss sie auch in der Strukturformel rechts stehen. Steht sie links, muss das auch in der Struktformel so realisiert sein.
Daher sind Strukturformeln von Zuckern keine einfachen Strukturformeln mehr, da sie zusätzliche Informationen über den geometrischen Aufbau enthalten. Man spricht daher von Projektionen, bzw. genauer von sogenannten Fischer Projektionen.
